Uncovering a root cause of the Growing Concern
Een groeiende
zorg
Genetische varianten in de melanocortine-4-receptor (MC4R) pathway kunnen de regulatie van honger, voedselinname, verzadiging en energieverbruik verstoren.1,2
Melanocortine-4-receptor & obesitas
Verstoorde MC4R-signalering kan leiden tot hyperfagie (onverzadigbare, pathologische honger) en ernstige, early-onset obesitas, ongeacht omgevings- en leefstijlfactoren.3,4
Er zijn meer dan 113 genen, die potentieel betrokken zijn bij de MC4R pathway; en zeldzame genetische varianten binnen de MC4R pathway kunnen resulteren in verminderde neuronale signalering, wat leidt tot zeldzame genetische ziekten zoals pro- opiomelanocortine (POMC) deficiëntie obesitas en leptine receptor (LEPR) deficiëntie obesitas.4,5
De onderliggende oorzaak niet gediagnosticeerd
De kernoorzaak van ernstige, early-onset obesitas wordt vaak ondergediagnosticeerd. Toegang tot de juiste hulpmiddelen en proactieve identificatie van klinische kenmerken kunnen helpen bij het stellen van de diagnose en mensen met een zeldzame MC4R-ziekte op het juiste zorgpad brengen.4,6
Heeft u een specifieke vraag?
Niet gevonden wat u zoekt of wilt u een onderwerp in meer detail bespreken? Neem contact op met ons team.Proactief, gepersonaliseerd obesitasmanagement
Prof. Luca Busetto bespreekt de noodzaak van proactief obesitasmanagement, waarbij de hoofdoorzaak van obesitas wordt geïdentificeerd en op een gepersonaliseerde manier wordt behandeld.[ENG]
Rhythm Pharmaceuticals is leveraging a IQVIA's Healthcare Professional Authentication solution to identify your eligibility to access this video content. If you already have an IQVIA account using it with other healthcare providers, please click 'Login' otherwise click 'Signup'.
Een zeldzame MC4R-pathway ziekte identificeren
Zodra de belangrijkste symptomen van hyperfagie en ernstige, early-onset obesitas zijn geïdentificeerd, kan genetische screening helpen bij het identificeren van de aanwezigheid van een zeldzame MC4R pathway ziekte..
Overweegt u of uw patiënt moet worden geëvalueerd voor een zeldzame MC4R pathway- ziekte? Denk dan aan de volgende cardinale symptomen:

Verhoogd en aanhoudend hongergevoel

Kortere periodes van verzadiging

Extreme preoccupatie met eten

Langere tijd nodig om verzadiging te bereiken

Aanzienlijke stress en ongepaste reacties als voedsel onthouden wordt

Buitensporig eetgedrag (nachtelijk eten, eten stelen, voedsel zoeken in het afval)
Ernstige, early-onset obesitas (early-onset is doorgaans voor de leeftijd van 5 jaar)
Een BMI-curve die ver boven de referentiepercentielen ligt, kan duiden op een onderliggende zeldzame MC4R pathway ziekte
Meer over de behandeling
Voor patiënten met een MC4R-pathway ziekte tikt de tijd


Sneller doorverwijzen
Er zijn een enkele cruciale klinische onderzoeken die moeten worden uitgevoerd voor de snelle identificatie van zeldzame MC4R pathway-ziekten:
- Het afnemen van een gedetailleerde klinische voorgeschiedenis is essentieel
- Vastleggen van de familiegeschiedenis, indien beschikbaar
Eerdere resistentie tegen traditionele strategieën voor obesitasmanagement kan een waardevol zijn om te mee te nemen in de afweging.
Hoewel individuele varianten zeldzaam zijn, zijn zeldzame MC4R pathway ziekten waarschijnlijk niet ongewoon bij mensen met ernstige, early-onset obesitas. De leeftijd waarop obesitas begint is een belangrijke factor bij het selecteren van patiënten met mogelijke varianten in obesitas-geassocieerde genen.
01
— 03
Kennisbank
Klik hier voor meer informatie over zeldzame MC4R pathway ziekten, educatiemateriaal en Rhythm gesponsorde sessies.
Deze pagina wordt regelmatig voorzien van nieuwe informatie over monogenetische obesitas en andere zeldzame MC4R pathway ziekten.
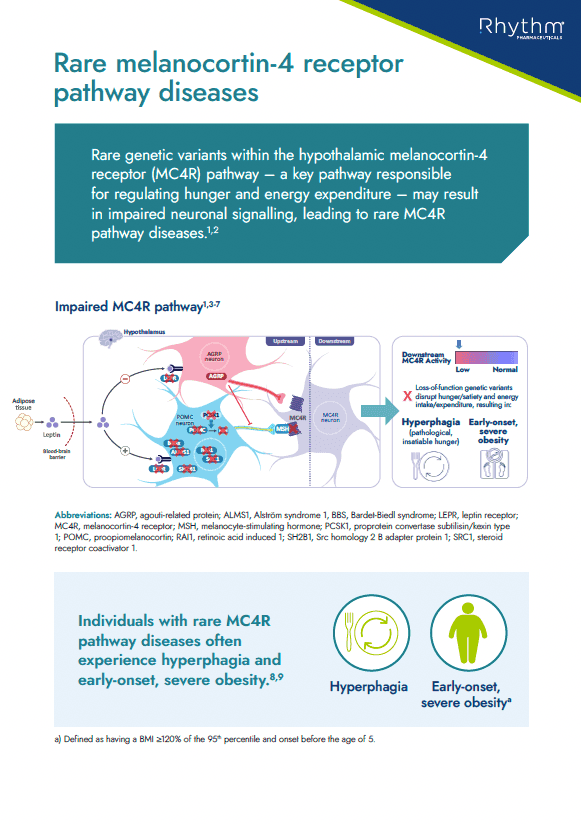
Educate HCPs on rare MC4R pathway diseases and how they can lead to hyperphagia and early-onset, severe obesity
Handout
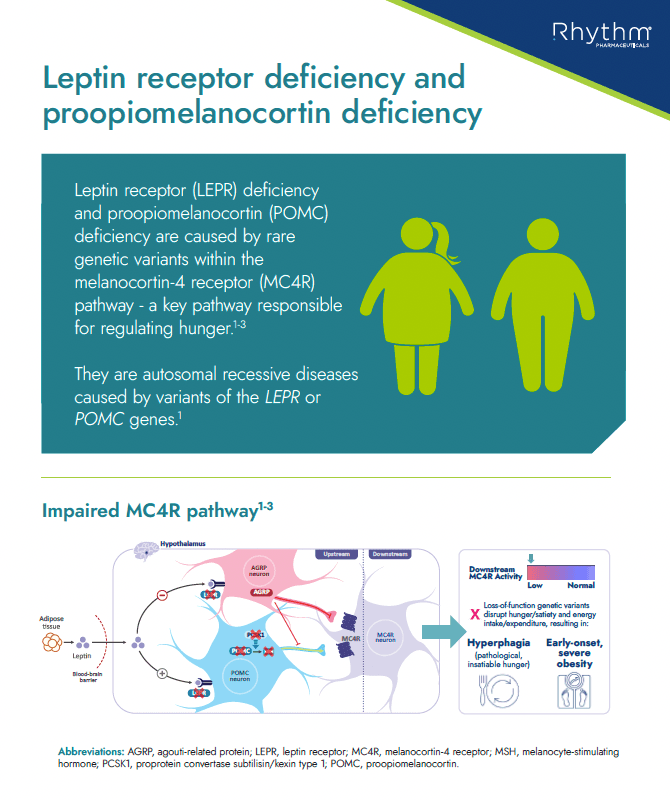
Educational information about LEPR and POMC deficiency, including what it is, key characteristics/clinical features in patients with these conditions, prevalence and route to diagnosis
Handout
Referenties:
- 1. Yazdi FT, et al. PeerJ. 2015;3:e856.
- 2. Acosta A, et al. Genes Nutr. 2014;9:384.
- 3. Haqq AM, et al. Lancet Diabetes Endocrinol. 2022;10(12):859–868.
- 4. Huvenne H, et al. Obes Facts. 2016;9:158–73
- 5. Fonseca ACP, et al. J Diabetes Complications. 2017;31:1549–1561.
- 6. Clément K, et al. Physiology Behavior. 2020;227:113134.
- 7. Styne DM, et al. J Clin Endocrinol Metab. 2017;102:709–757.
- 8. Heymsfield SB, et al. Obesity (Silver Spring). 2014;22:S1‒S17.
- 9. Ellacott KLJ & Cone RD. Philos Trans R Soc Lond B Biol Sci. 2006;361:1265–74.
- 10. Kohldorf K, et al. Int J Obes (Lond). 2018;42:1602–1609.
- 11. August GP, et al. J Clin Endocrinol Metab. 2008;93:4576–99.
- 12. Kleinendorst L, et al. BMJ Case Rep. 2017;2017:bcr2017221067.