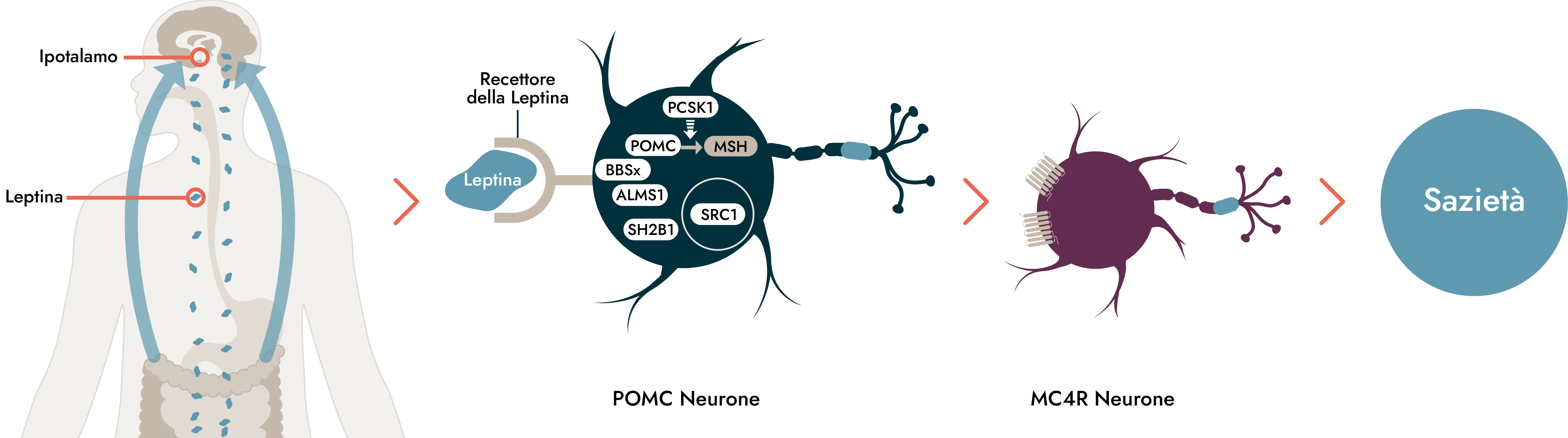
Il pathway del MC4R ha un ruolo fondamentale nel meccanismo di regolazione della fame, che comporta l'attivazione dei neuroni ipotalamici in risposta alla produzione di leptina dalle cellule del tessuto adiposo. Per una corretta regolazione del senso di fame occorre avere livelli sufficienti di specifici neuropeptidi, l'ormone a-melanocito-stimolante (a-MSH), che attivano l'MC4R determinando una diminuzione della fame e il contemporaneo aumento del dispendio energetico.1,2,6